Compilação com os melhores mapas mentais, conceituais, infográficos, diagramas e resumos sobre propriedades periódicas.
Mapa Mental sobre propriedades periódicas (1)
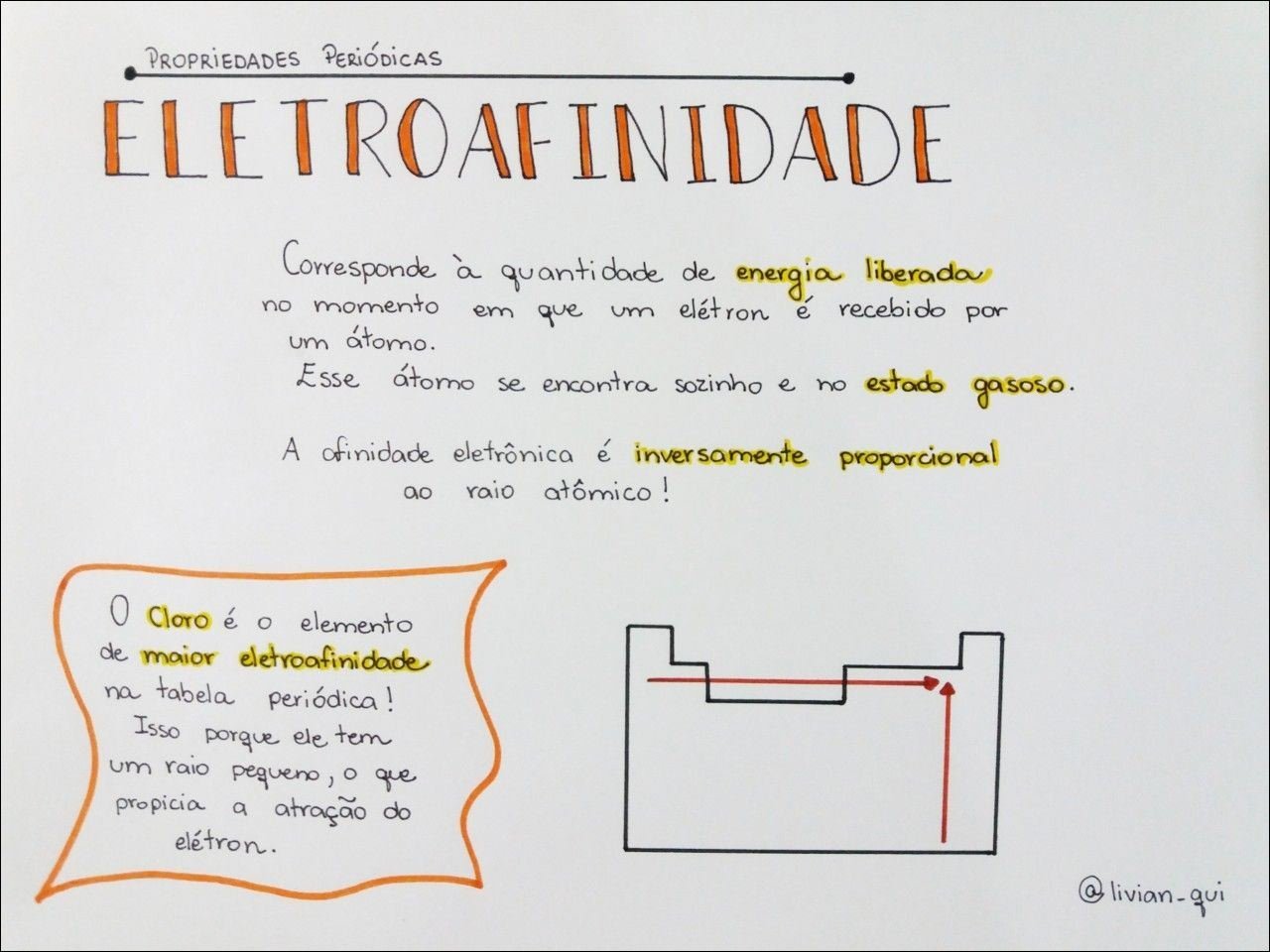
Mapa Mental sobre propriedades periódicas (2)
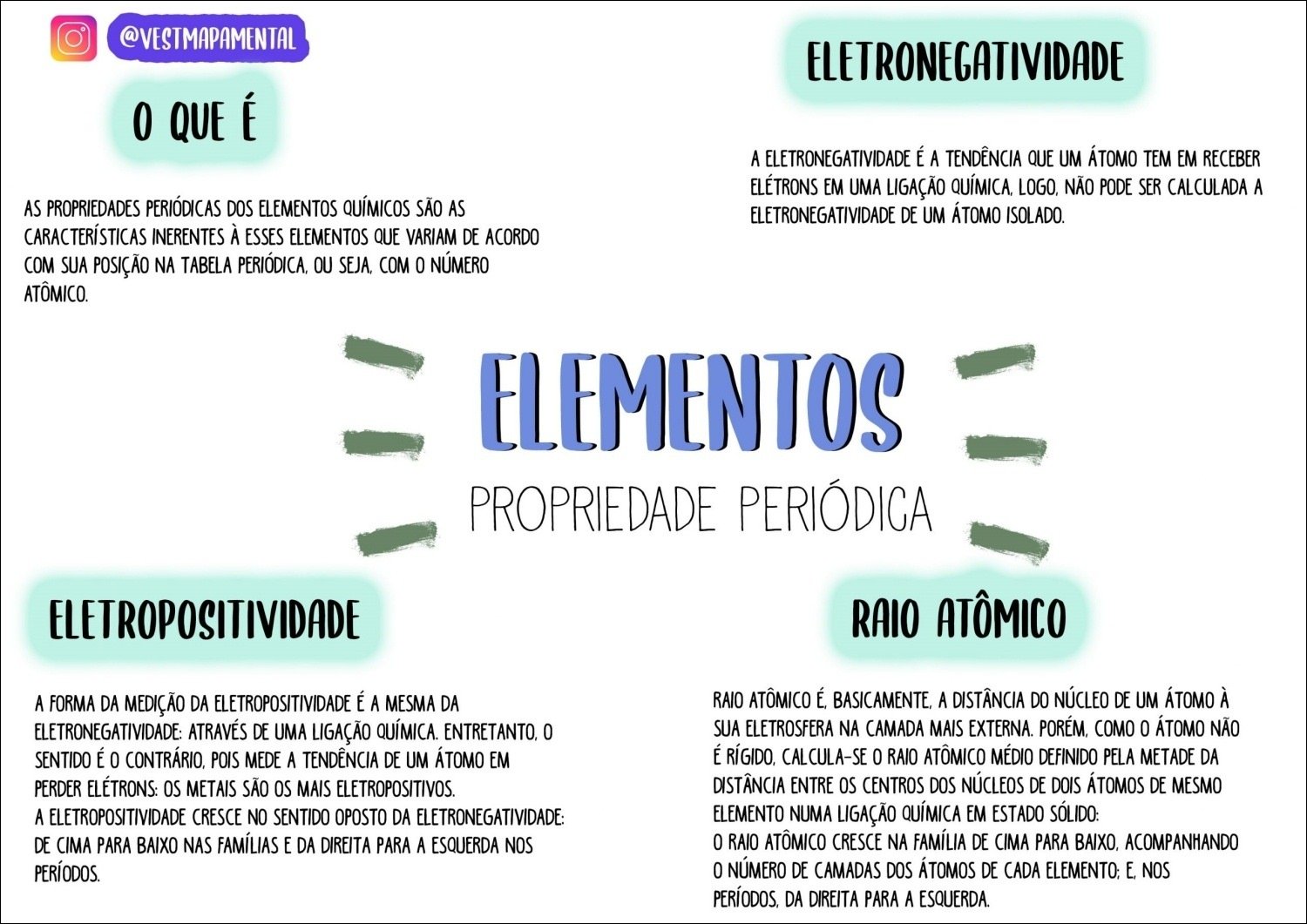
Mapa Mental sobre propriedades periódicas (3)
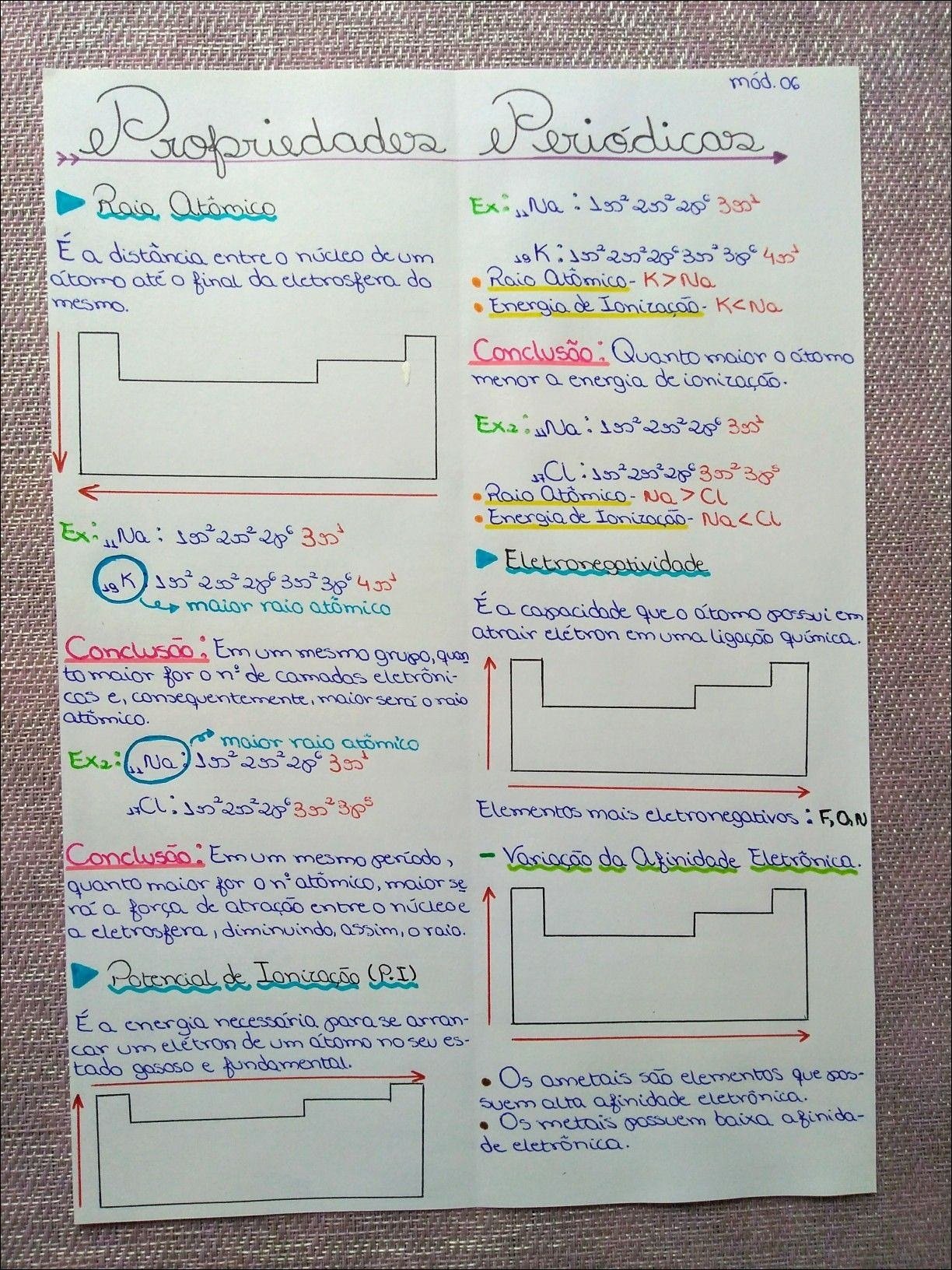
Mapa Mental sobre propriedades periódicas (4)

Mapa Mental sobre propriedades periódicas (5)

Mapa Mental sobre propriedades periódicas (6)
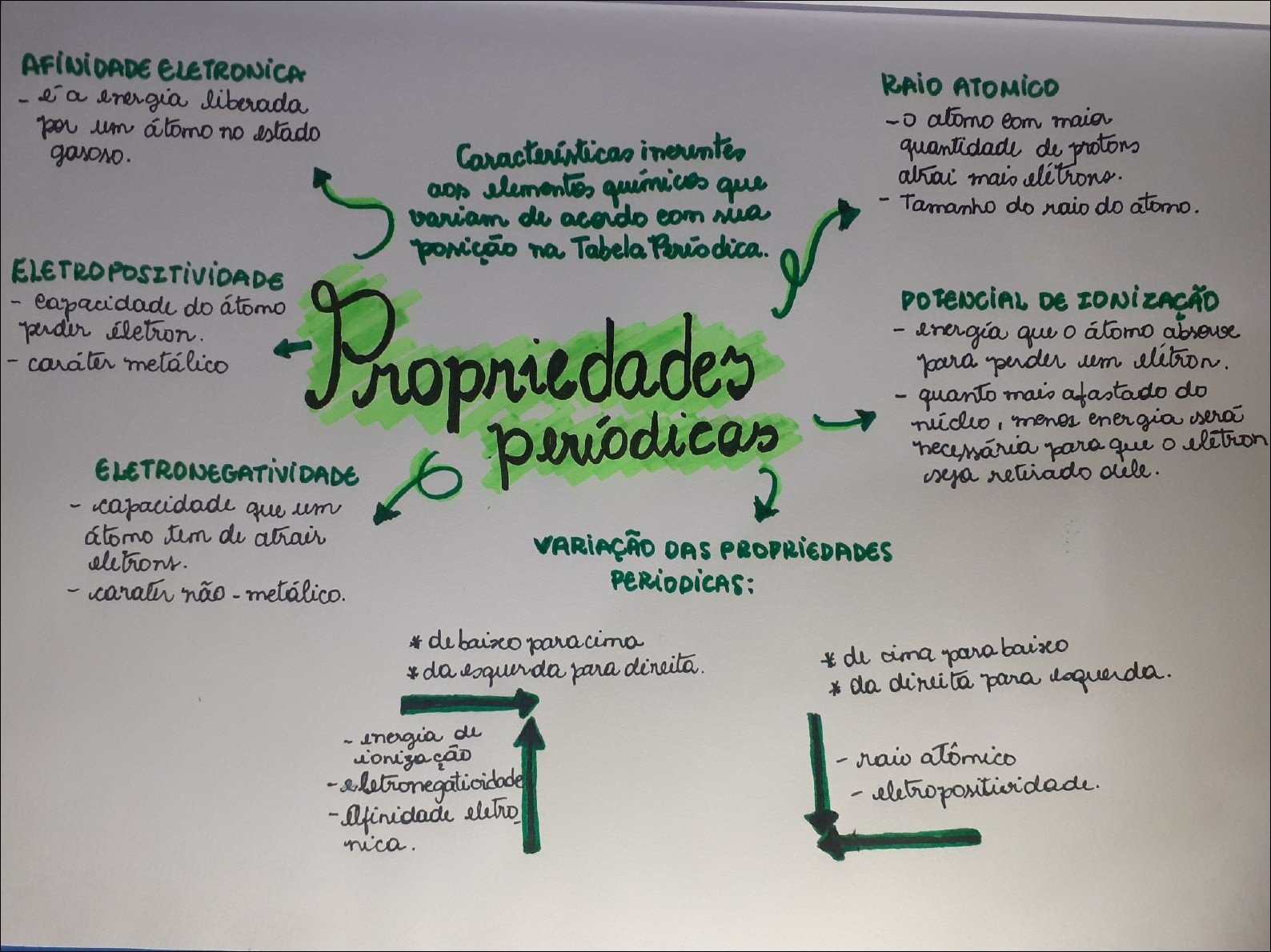
Mapa Mental sobre propriedades periódicas (7)
Mapa Mental sobre propriedades periódicas (8)
Mapa Mental sobre propriedades periódicas (9)
Mapa Mental sobre propriedades periódicas (10)
Mapa Mental sobre propriedades periódicas (11)

Mapa Mental sobre propriedades periódicas (12)
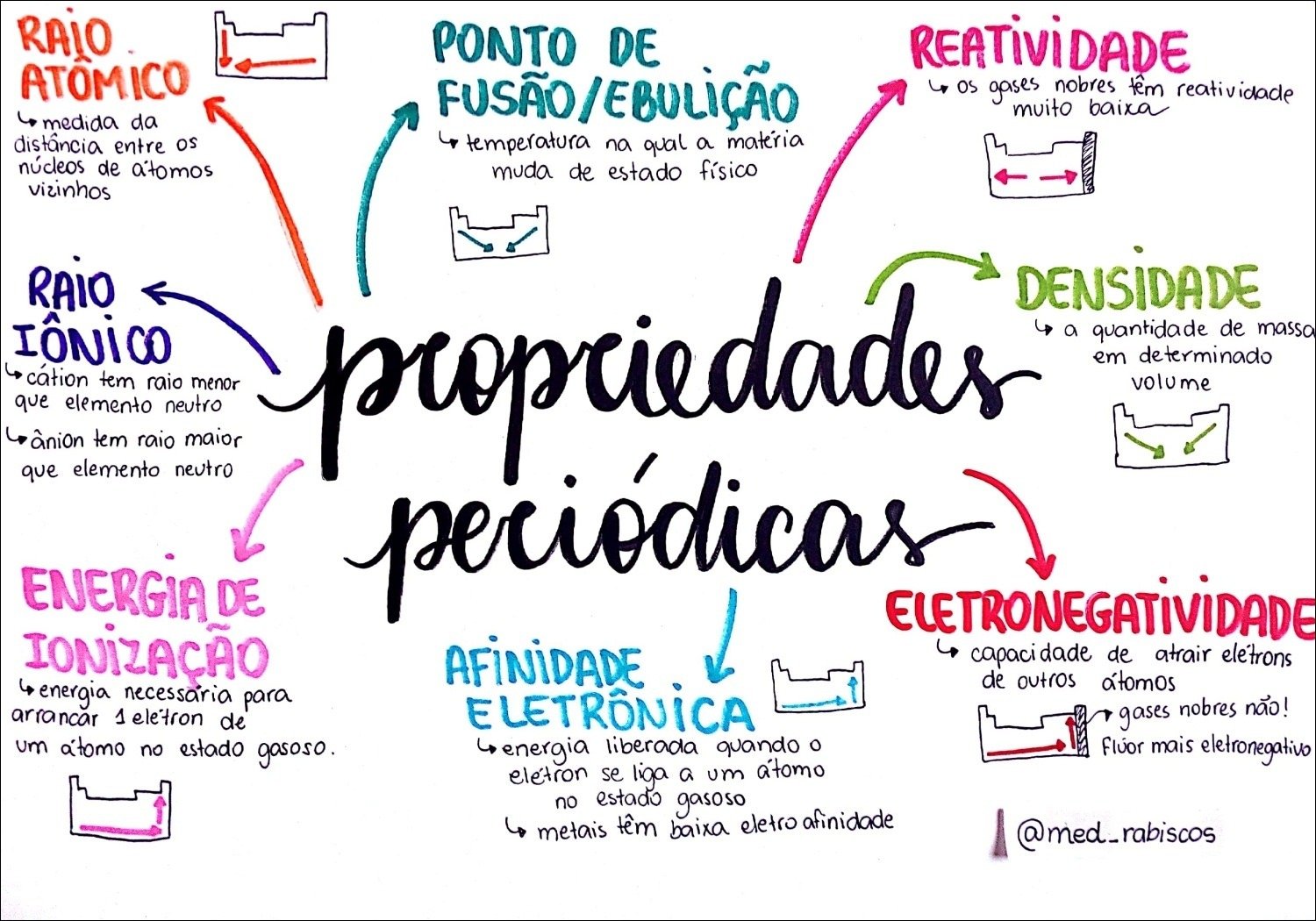
Mapa Mental sobre propriedades periódicas (13)
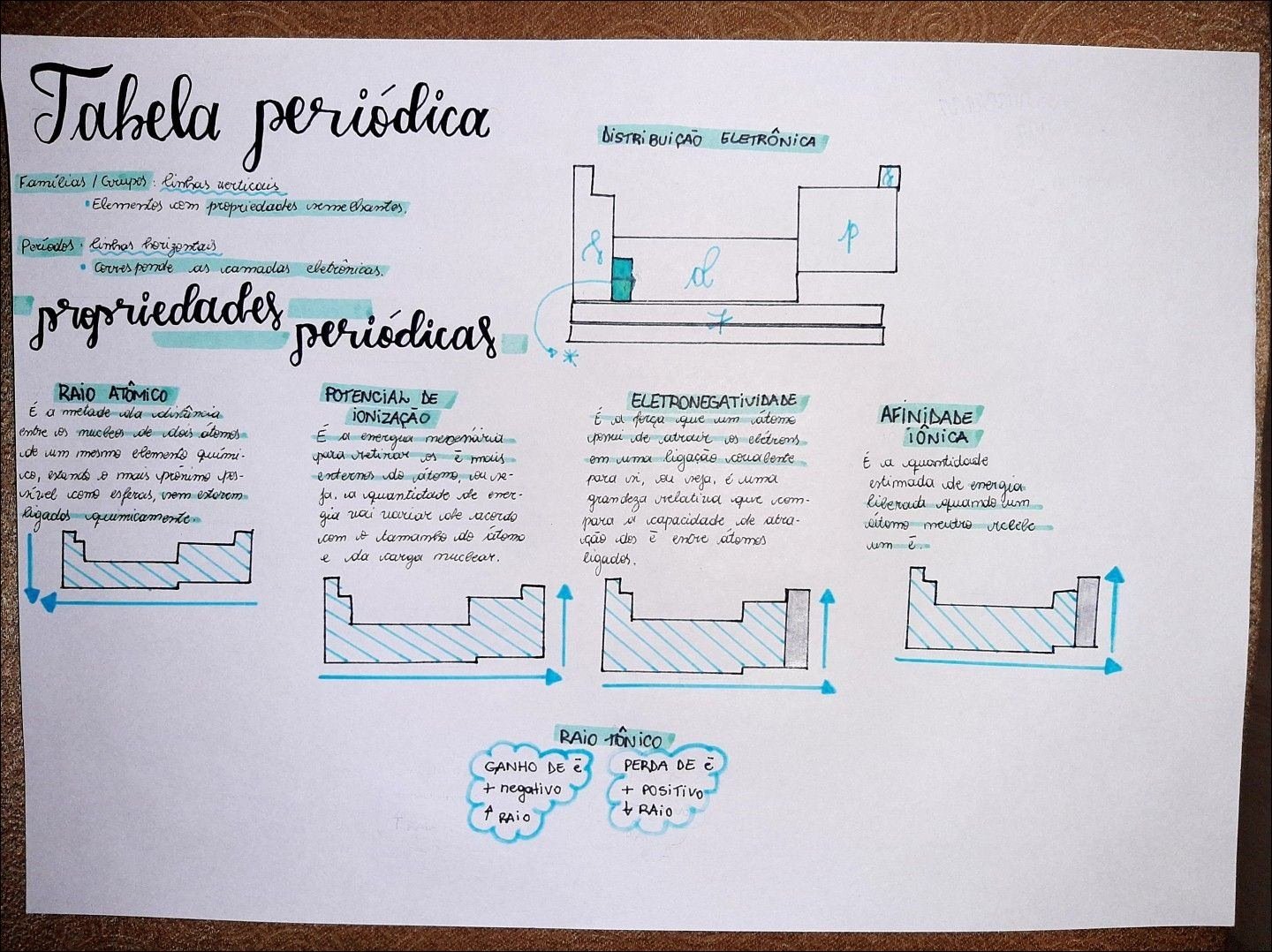
Mapa Mental sobre propriedades periódicas (14)
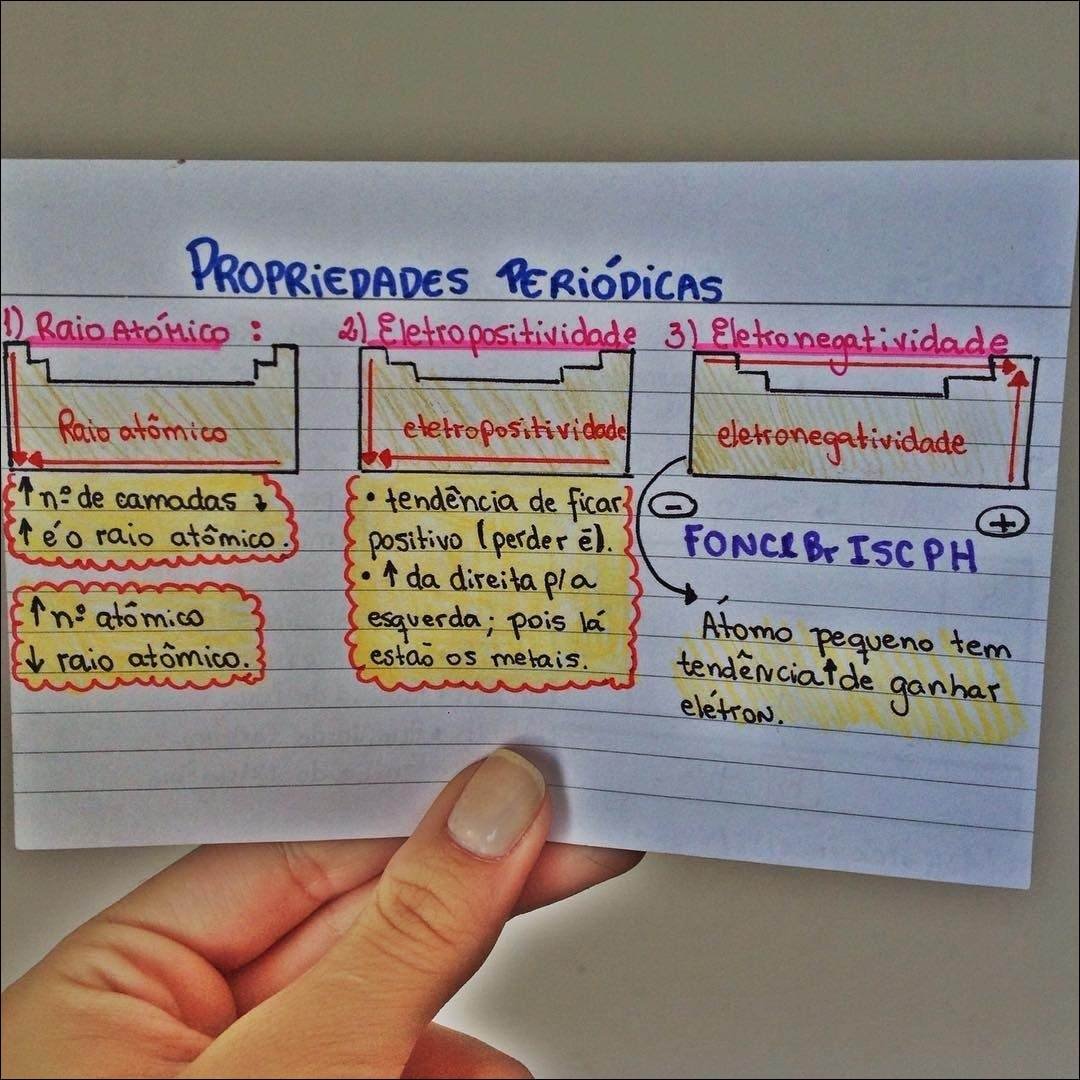
Mapa Mental sobre propriedades periódicas (15)

Mapa Mental sobre propriedades periódicas (16)

Mapa Mental sobre propriedades periódicas (17)
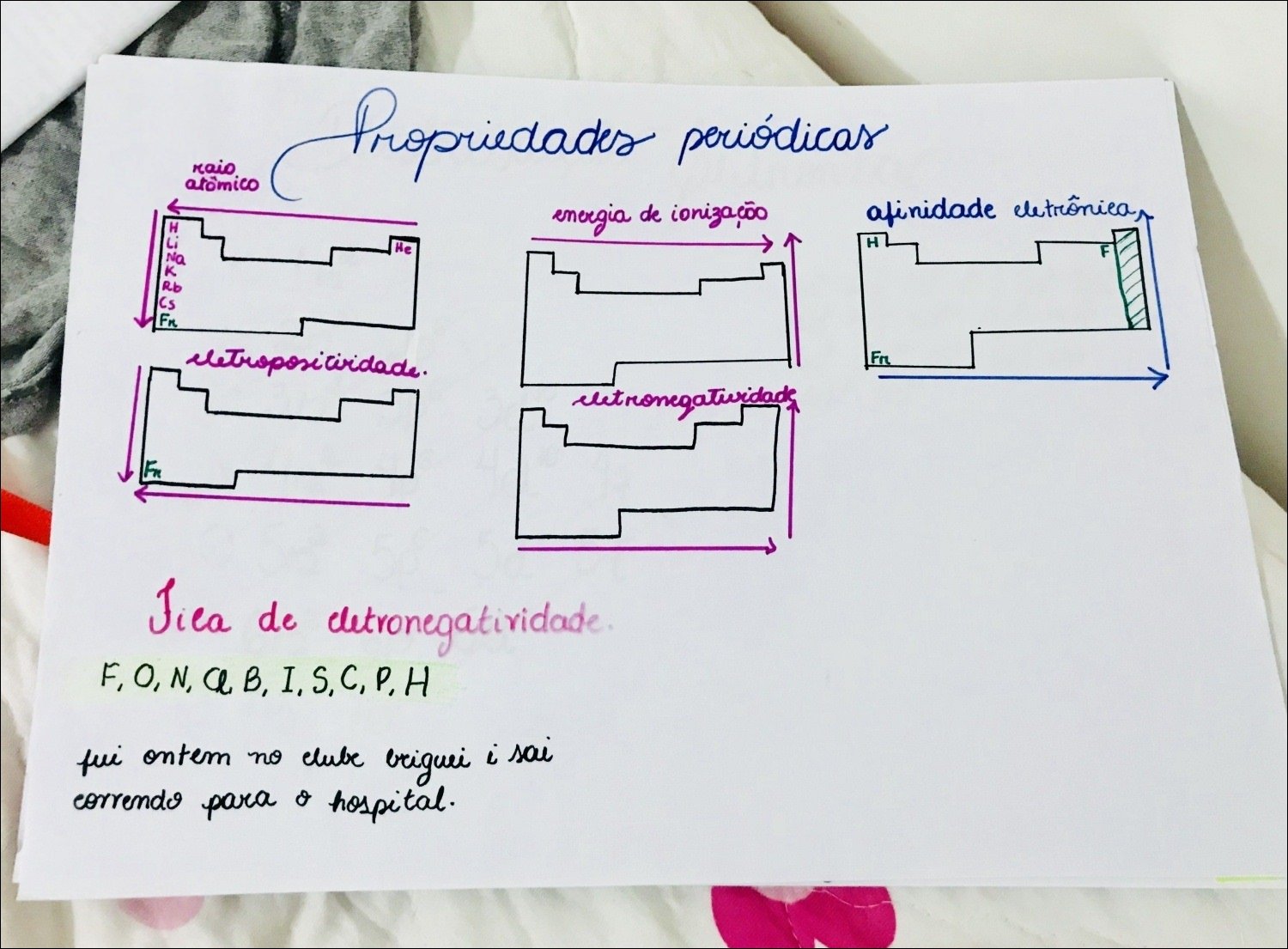
Resumo sobre propriedades periódicas
As propriedades periódicas são as características dos elementos químicos que variam de forma previsível e regular com base na sua posição na Tabela Periódica. Essa periodicidade decorre da configuração eletrônica dos átomos, que se organiza de forma repetitiva e organizada.
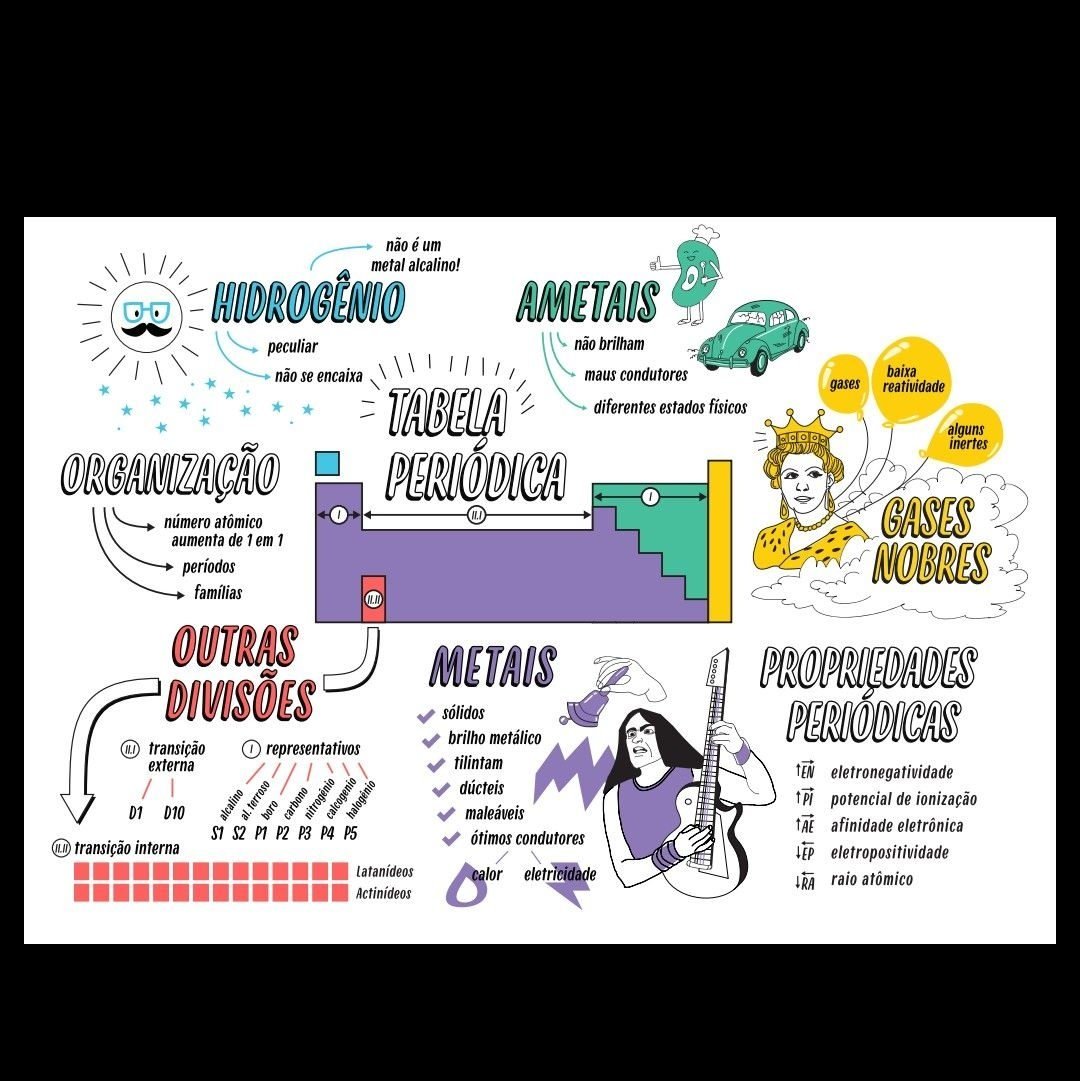
As principais propriedades periódicas incluem:
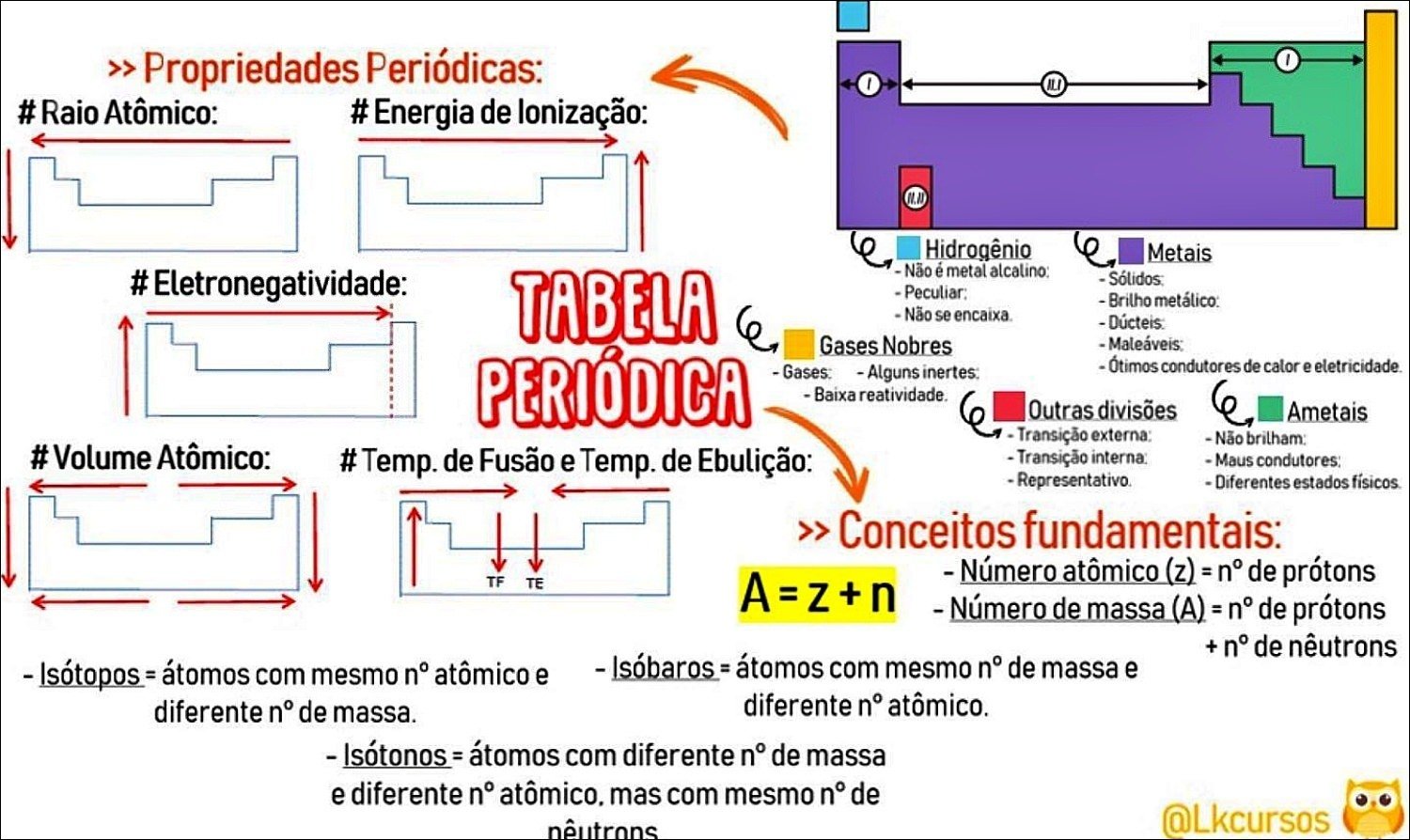
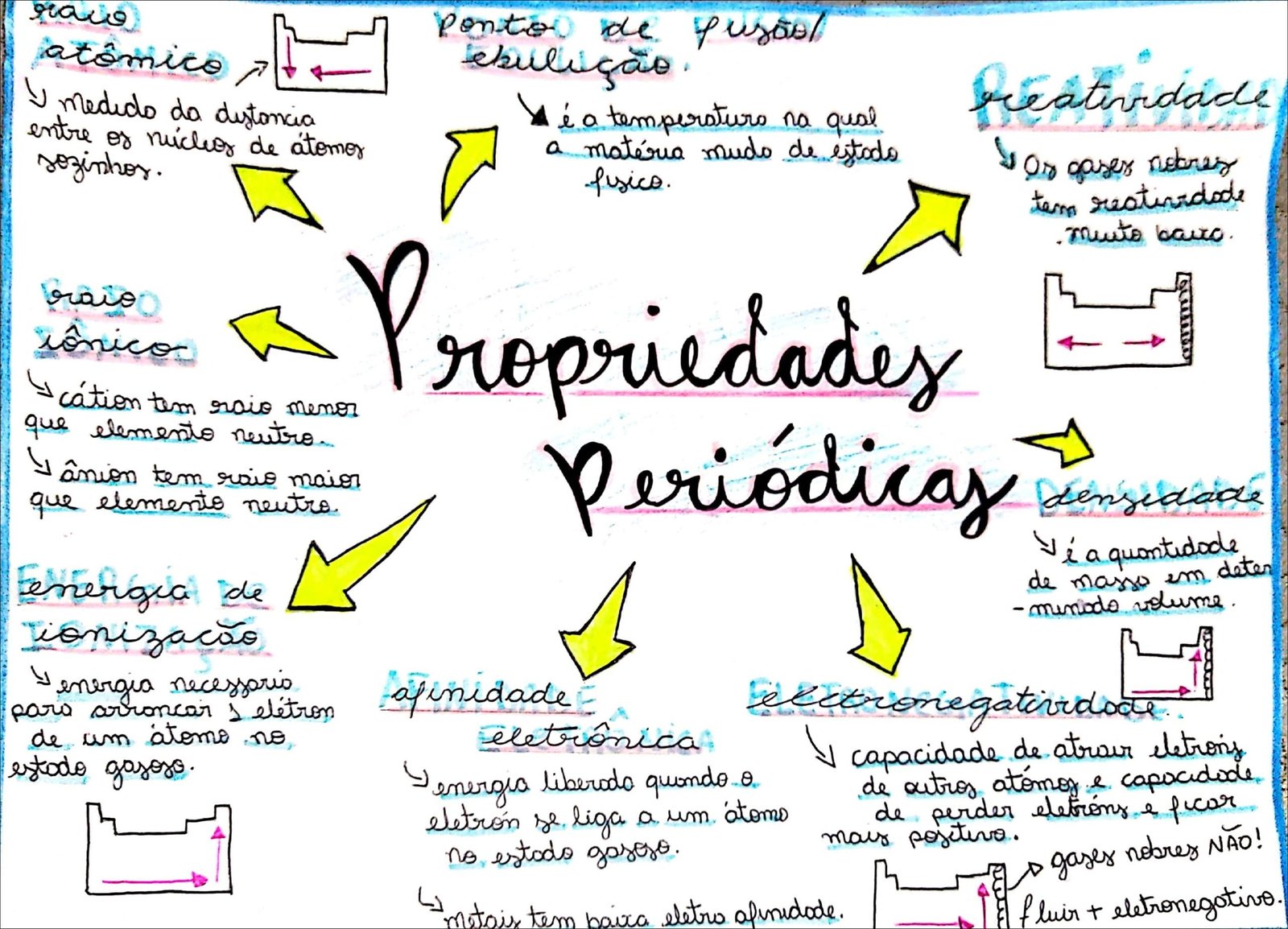
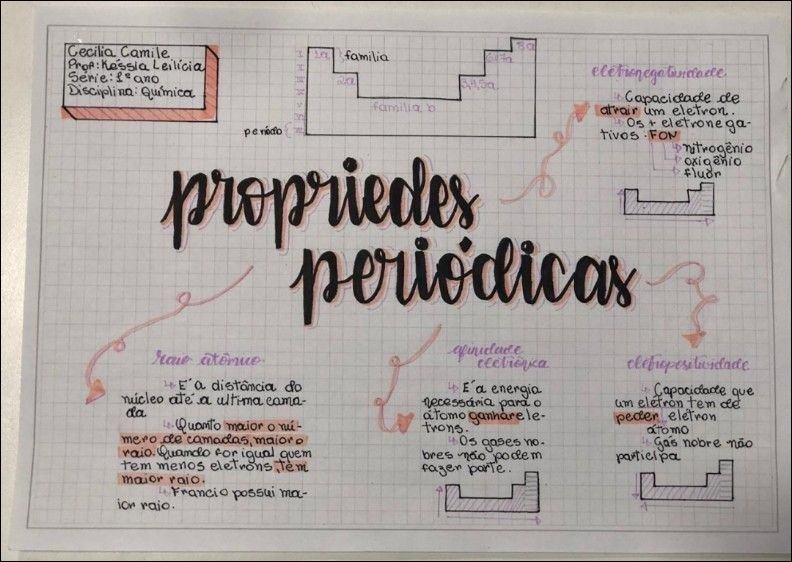
- Raio Atômico: A metade da distância entre os núcleos de dois átomos idênticos ligados entre si. Diminui de baixo para cima e da esquerda para a direita na tabela, devido ao aumento da atração nuclear e da força de Coulomb.
- Energia de Ionização: A energia necessária para remover um elétron de um átomo no estado gasoso. Aumenta de baixo para cima e da esquerda para a direita, pois os elétrons estão mais próximos do núcleo e sentem maior atração.
- Afinidade Eletrônica: A variação de energia quando um elétron é adicionado a um átomo no estado gasoso. Geralmente aumenta de baixo para cima e da esquerda para a direita.
- Eletronegatividade: A capacidade de um átomo atrair elétrons em uma ligação química. Aumenta de baixo para cima e da esquerda para a direita, refletindo a força com que um átomo atrai elétrons.
- Caráter Metálico: A tendência de um elemento em perder elétrons e formar cátions. Diminui de baixo para cima e da esquerda para a direita.
Compreender as propriedades periódicas é essencial para prever o comportamento químico dos elementos, suas reações e as propriedades dos compostos que formam. Ao analisar as tendências na Tabela Periódica, os químicos podem estimar as propriedades desconhecidas e entender as relações entre estrutura atômica e as características observáveis da matéria.
